SAFEST-prosjektet
Siden august 2021 har jeg jobbet på SAFEST-prosjektet hos Direktoratet for medisinske produkter (DMP) (tidligere Statens Legemiddelverk1). Formålet med prosjektet var opprinnelig å etablere en kilde til strukturert legemiddelinformasjon som understøtter behovene i sykehus. Men i en rapport fra Helsedirektoratet (tidligere Direktoratet for e-helse2) som skulle vurdere den strategiske retningen for en kilde til felles legemiddelgrunndata, blir SAFEST-prosjektet trukket frem som en viktig del av målarkitekturen og den strategiske retningen for felles legemiddelgrunndata3.
Bakgrunn
Mye av bakgrunnen for dette prosjektet er behovet for å gå over til internasjonale standarder, som er avgjørende for et effektivt leverandørmarked og internasjonal samhandling. Norge er ganske tidlig ute med dette, noe som blir lagt merke til utenfor landegrensene.
Grunnen til at SAFEST-prosjektet blir trukket frem av Helsedirektoratet, er på grunn av verdien dataene som leveres i prosjektet kan tilby. Målarkitekturen som de presenterer, beskriver følgende forhold rundt en nasjonal tjeneste:
- Felles informasjonsmodell for legemiddelgrunndata basert på ISO IDMP og felles informasjonsmodell for deling i verdikjeden basert på ressurser i FHIR.
- Standardiserte og åpne grensesnitt for utveksling og distribusjon av legemiddelgrunndata skjer med API’er basert på FHIR.
- Teknisk løsning som legger til rette for effektiv sentral informasjonsforvaltning og utveksling av data fra ulike produsenter og til konsumenter. Løsningene fra SAFEST-prosjektet kan ligge til grunn for komponenter i en teknisk løsning.
- Definerte roller og ansvar der produsenter, konsumenter og integrator inngår i leveranse og forvaltningskjeden for grunndata, og en overordnet koordinering av behov og tiltak.
Det blir også trukket frem i rapporten at helsesektoren i Norge i all hovedsak støtter dette forslaget til målarkitektur og et ønske om å gå i denne retningen.
Key Innovator
SAFEST-prosjektet er med på å understøtte implementering og utbredelse av en felles standard på medisinske produkter og det er derfor Norge har blitt trukket frem av EU-kommisjonens «Innovation Radar» som en «Key Innovator»4.
Teknisk implementasjon
I all hovedsak består den tekniske løsningen av 4 hovedkomponenter.
- Dataoverføringsmodulen hostes i Microsoft Azure.
- Kvalitetsforbedringsmodulen, med transformasjon til FHIR-format og -struktur, betjenes av pipelines i Sesam.
- Kvalitetskontrollprosessene håndteres gjennom GUI i Microsoft Dynamics 365.
- Distribusjonsmodulen hostes i Microsoft Azure.
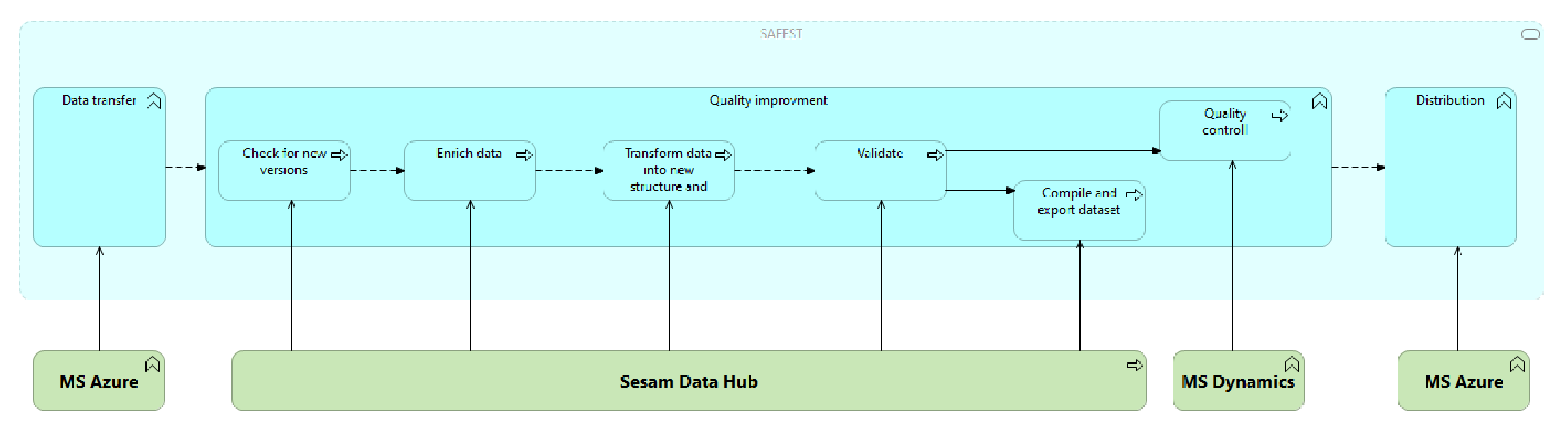
Det har også blitt utviklet et omfattende test-rammeverk for å validere dataene som blir publisert i FHIR API-et, dette for å sikre at pasientsikkerheten er ivaretatt når aktører skal ta dataene i bruk.